第五期CRISPR诊断技术的创新与转化——ToloBio王金:CRISPR-based Non-nucleic Acid Detection
CRISPR-Cas 系统是原核生物的适应性免疫系统,其精准识别与高效切割特性被广泛应用于基因编辑与分子诊断。王金博士团队首次鉴定 CRISPR-Cas12 蛋白的反式切割活性,并开发 HOLMES™ CRISPR 分子诊断系统,推动了 CRISPR 诊断技术的发展。传统 CRISPR 检测以核酸为主要靶标,在病原体检测、肿瘤液体活检等领域具备临床应用潜力。
然而,临床与现场快速检测中大量关键标志物为非核酸靶标,包括蛋白质、小分子代谢物、金属离子、酶活性等,开发基于 CRISPR 的非核酸检测技术具有重要临床价值与应用前景。

王金博士,吐露港生物创始人、CEO,中国医药生物技术协会生物诊断技术分会常务委员。主要研究方向是基于CRISPR原理的“下一代分子诊断技术的开发及其应用”。首次鉴定CRISPR-Cas12蛋白的反式切割活性,并开发了名为“HOLMES/福尔摩斯”的新型CRISPR分子诊断系统。
以下为王金博士的部分报告内容:
注:报告由生物诊断平台整理汇编,内容仅供学习参考。
01
1.1 反式切割活性
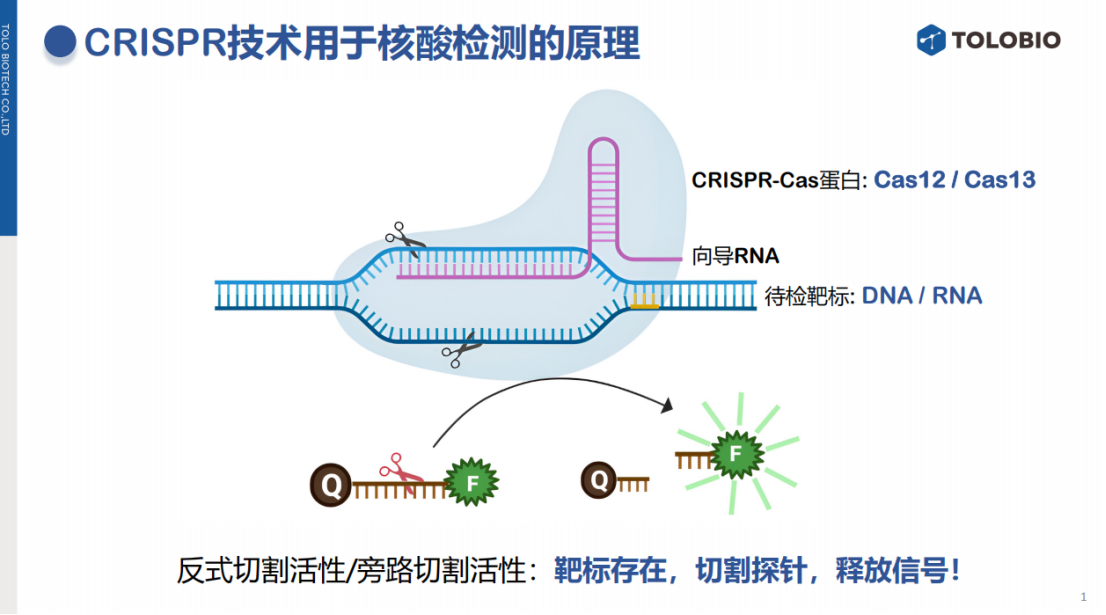
CRISPR诊断技术的核心在于特定Cas蛋白(如Cas12、Cas13)的反式切割活性(也称旁路切割活性)。在向导RNA(crRNA)的引导下,Cas蛋白能够精准识别并结合靶标核酸,形成三元复合物。该过程不仅能顺式切割靶标核酸,更重要的是能激发Cas蛋白对体系中任意单链核酸探针的非特异性、高效切割,从而释放出可检测的信号。
1.2 技术优势
与传统分子诊断技术(如qPCR)相比,基于CRISPR的诊断系统具备三大核心优势:
高特异性:Cas蛋白在crRNA引导下识别靶标,具有单碱基分辨率的特异性,能有效区分SNP。
高灵敏度:一旦被激活,一个Cas蛋白可以切割成千上万个报告探针,实现信号的指数级放大。结合靶标预扩增步骤,其灵敏度可达单分子(aM)水平,有效降低假阴性率。
操作简便:整个反应在恒温条件下进行,无需PCR仪那样精密的变温设备。这使得CRISPR技术尤其适用于家庭自测、现场快速检测(POC)等场景,仅需低成本、便携式的小型加热设备即可完成。

02
2.1 技术核心逻辑
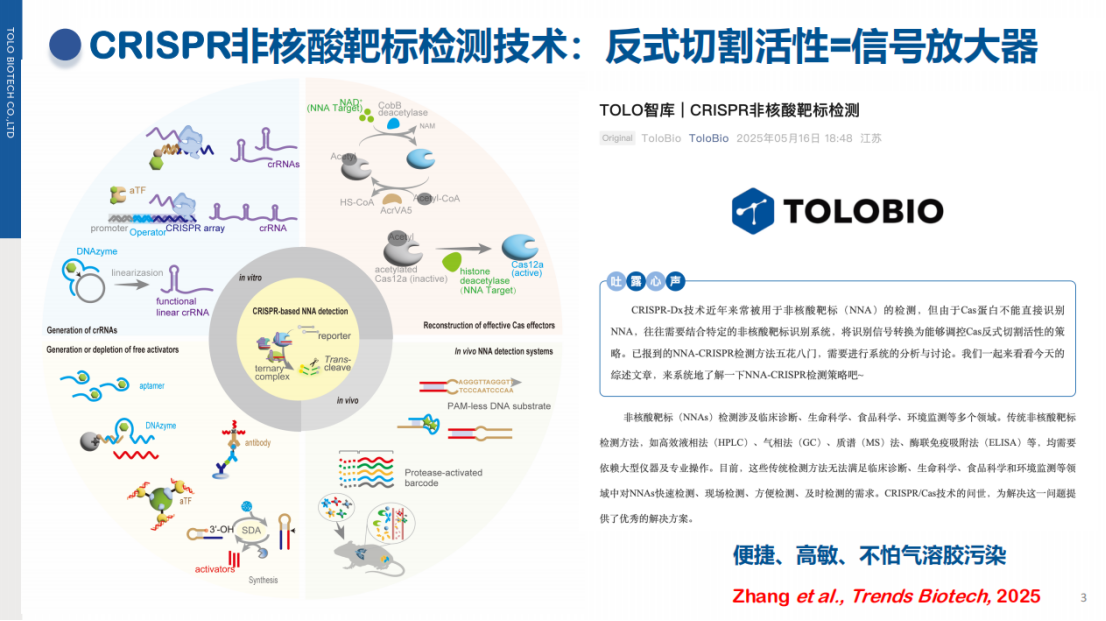
将CRISPR技术应用于非核酸靶标(如小分子、蛋白、激素等)检测时,其反式切割活性依然充当信号放大器的角色。然而,由于Cas蛋白本身只识别核酸,需通过耦联识别系统将非核酸信号转化为可调控 Cas 反式切割活性的分子事件。
CRISPR 用于非核酸检测时,除了信号放大,灵敏度高以外,还有几个优点:
1.不怕气溶胶污染:免扩增检测非核酸靶标。
2.恒温便捷:保持 CRISPR 技术现场检测优势
2.2 激活子释放策略
2.2.1 基于变构转录因子(aTF)的检测
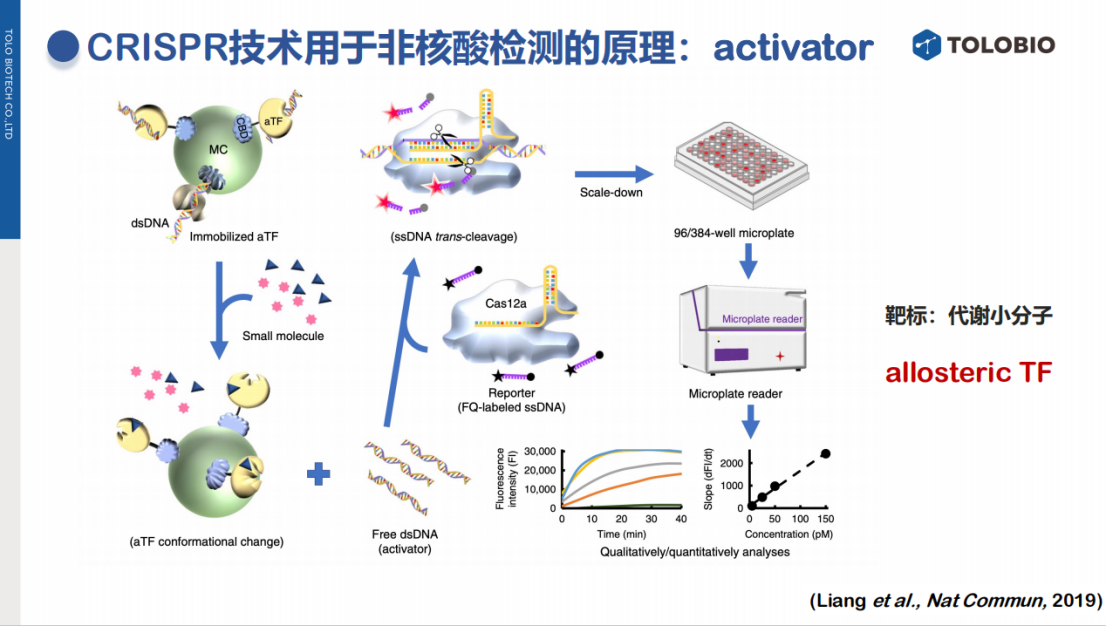
此方法利用变构转录因子(aTF)作为分子开关。aTF能特异性结合一段DNA序列。当待检测的小分子靶标存在时,它会与aTF结合,导致aTF从DNA上解离下来,从而释放出原本被结合的核酸序列。该游离的核酸序列即可作为Activator,被CRISPR系统识别,激活Cas蛋白并产生信号。
2.2.2 基于适配体的检测
适配体(Aptamer)是能特异性结合靶标的单链DNA或RNA。在该设计中,适配体首先与Activator结合形成复合物,使其处于封闭状态。当待检测的靶标分子(如小分子、金属离子)存在时,适配体会优先与靶标结合,从而释放出游离的Activator。随后,该Activator激活CRISPR-Cas系统,切割探针并输出信号。
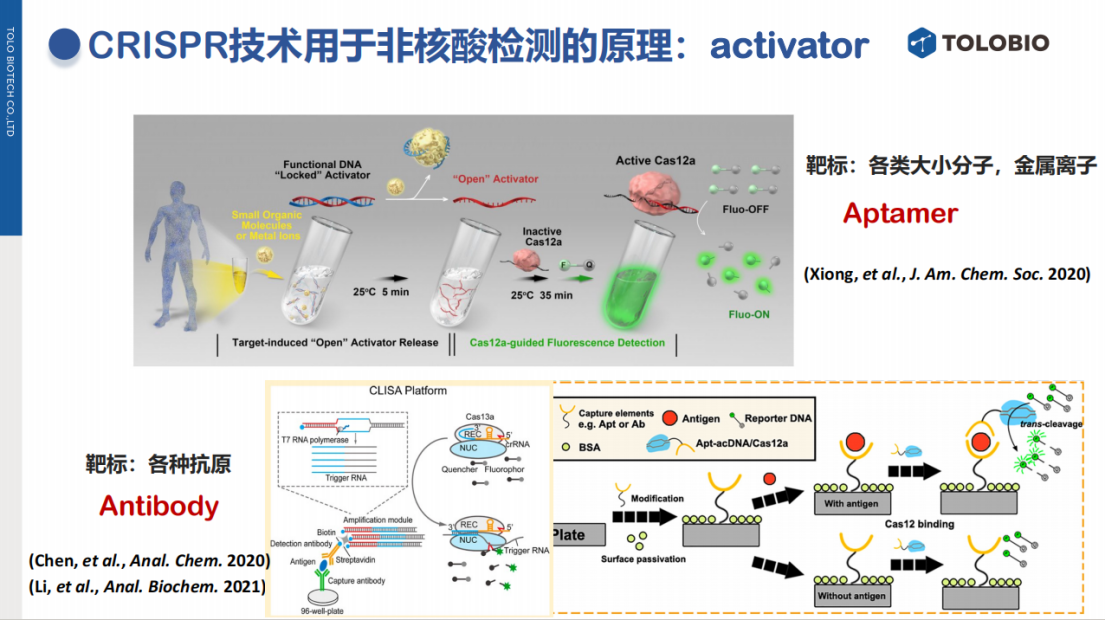
2.2.3 基于CRISPR-ELISA (CLISA) 的免疫检测
针对蛋白质等大分子靶标,可将CRISPR技术与传统ELISA原理结合。该方法使用捕获抗体和检测抗体(其上偶联了特定的核酸Activator)对抗原采用“三明治”双抗夹心法进行检测。当抗原存在时,检测抗体被保留,其携带的Activator将激活CRISPR反应,切割探针。相较于传统ELISA或化学发光的信号输出方式,CRISPR的信号放大能力可以显著提升免疫检测的灵敏度,具有突破现有技术瓶颈的潜力。
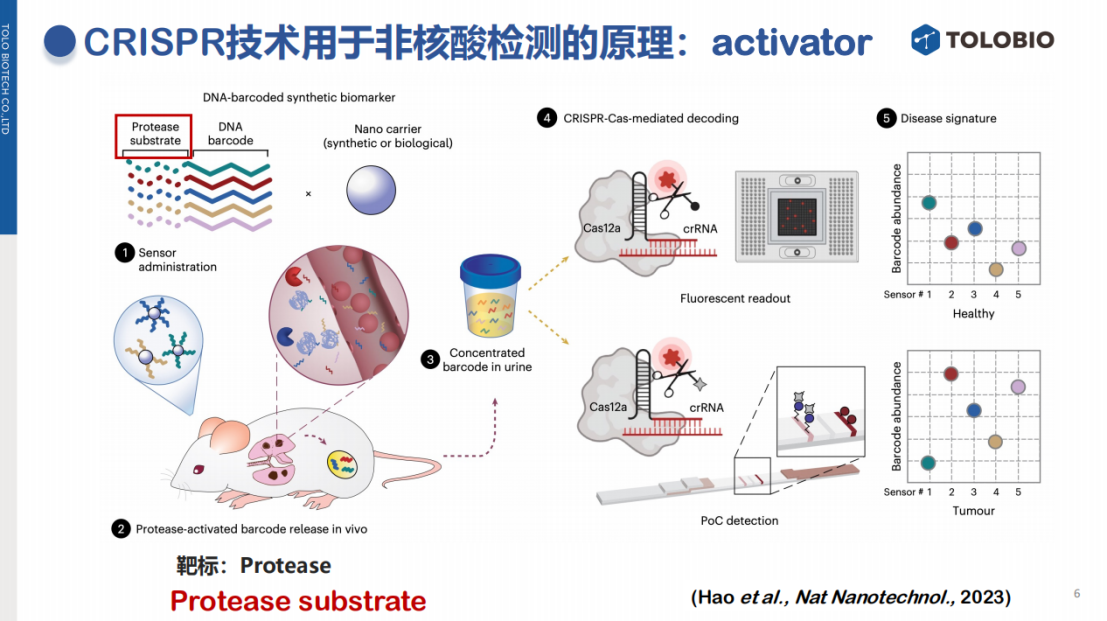
除了产生Activator,CRISPR系统的激活还可以在向导RNA(gRNA)和Cas蛋白本身等关键节点进行调控。
2.3 调控gRNA的生成
可通过设计特定的分子机制,使功能性gRNA的产生依赖于靶标的存在。
gRNA转录调控:利用变构转录因子(aTF)调控gRNA的转录模板。靶标存在可使aTF解离,从而允许T7 RNA聚合酶转录出具有功能的gRNA,进而激活Cas蛋白。
环状gRNA的激活:设计一个环状的、无活性的前体gRNA。当特定配体(靶标)存在时,会激活一个核酶,该核酶将环状gRNA切割成有功能的线性gRNA,从而启动CRISPR反应。
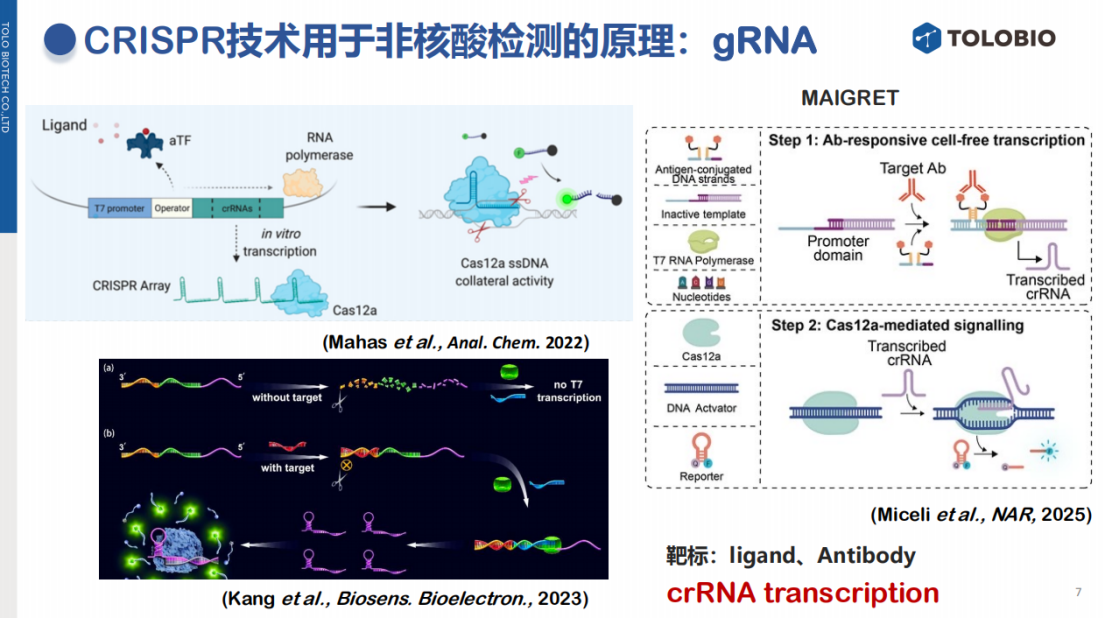
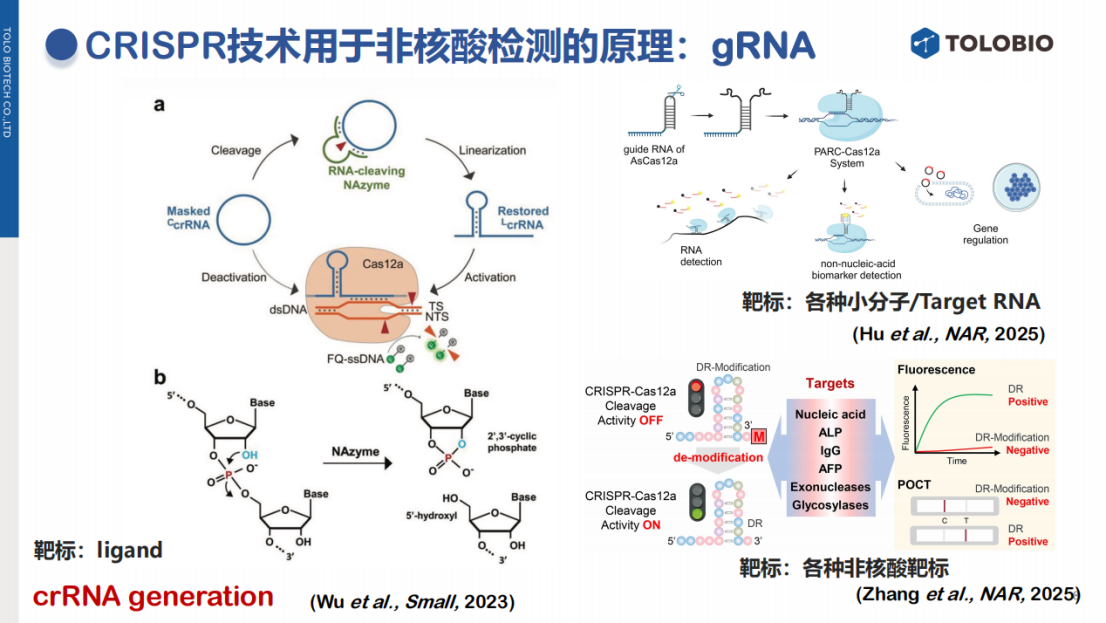
2.4 调控Cas蛋白的活性
自然界中,宿主与噬菌体的博弈提供了精妙的调控范例。研究发现,Cas蛋白的活性可被翻译后修饰(如乙酰化)所调控。
基于此原理,可构建依赖辅酶因子NAD+的检测系统。在该系统中,Cas蛋白被预先乙酰化而失活。只有当体系中存在NAD+时,去乙酰化酶(如CobB)才能被激活,进而对失活的Cas蛋白进行去乙酰化,恢复其反式切割活性并产生信号。
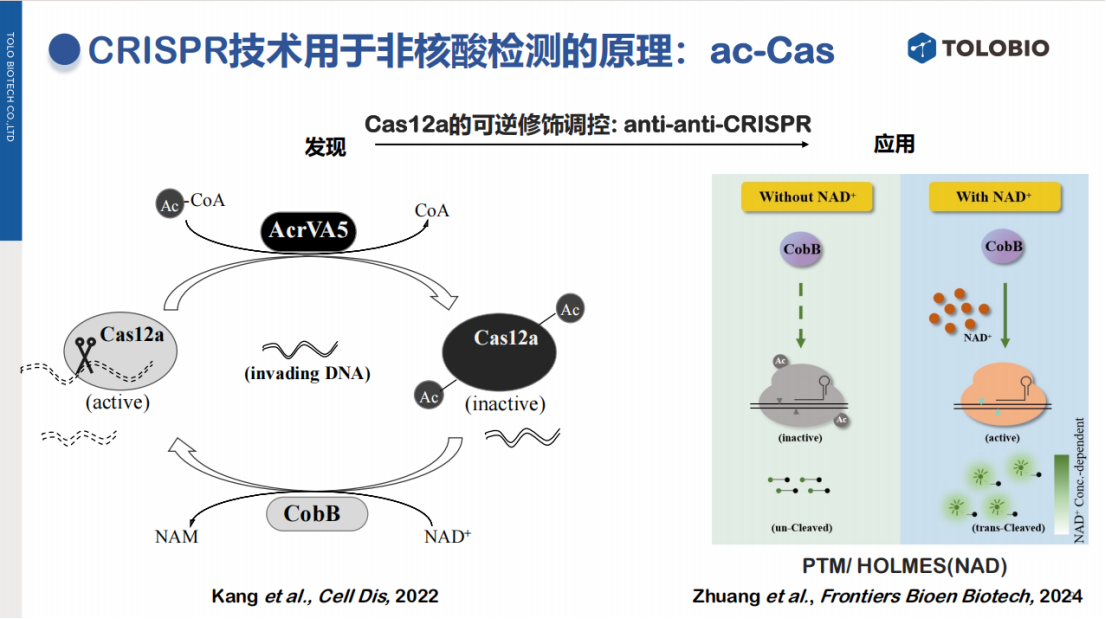
2.5 Split-Cas系统
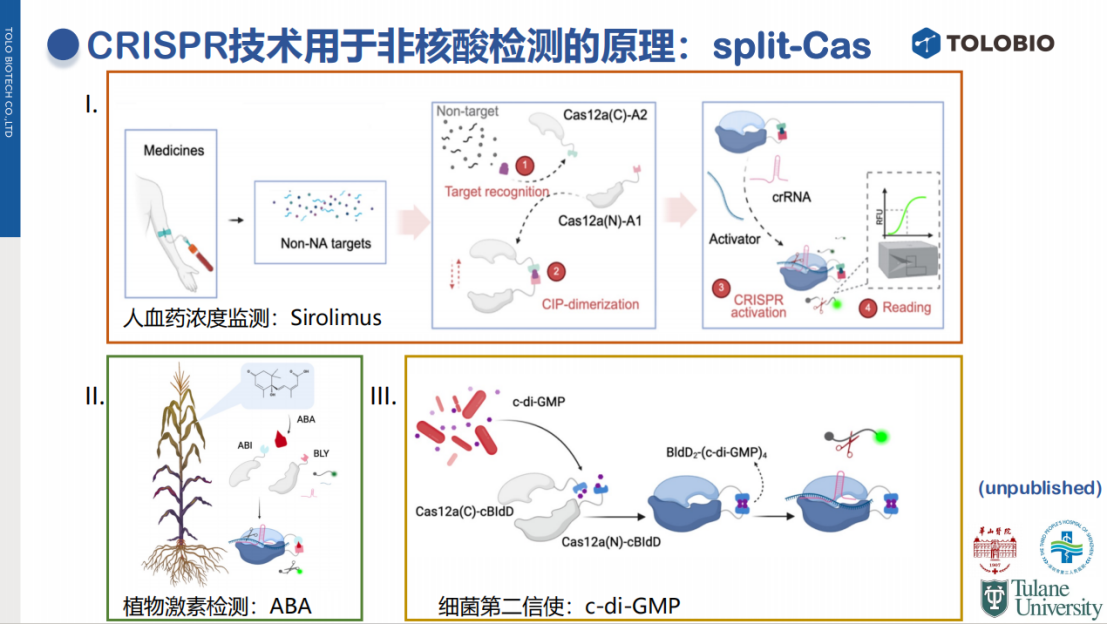
吐露港基于split-Cas12a开发了一种通用的非核酸靶标检测平台,旨在实现针对任意靶标的均相、免洗检测。
核心技术:将Cas蛋白拆分为无活性的N和C两段结构域,分别融合一个能与特定靶标结合的一组蛋白结构域。
工作原理:当待测靶标(如小分子、激素)存在时,它会分别结合耦联的靶标结合结构域,进而将分裂(split)的Cas蛋白拉到一起,形成有活性的Cas蛋白,高效切割报告探针并释放信号。
应用案例:
人血药浓度监测(雷帕霉素):利用雷帕霉素天然结合的FKBP和FRB结构域,构建的Split-Cas系统可以1-2微升指尖血为样本,在10分钟内完成检测。与质谱或化学发光法相比,该方法更快、更简便、成本更低,在200例临床样本中的符合率达到100%。
植物激素检测(脱落酸ABA):通过更换为ABA响应的结合域,该系统同样可用于植物激素的快速检测。
细菌第二信使检测(c-di-GMP):通过设计c-di-GMP响应的结合域,实现对该信号分子的检测。
03
4.1 行业痛点
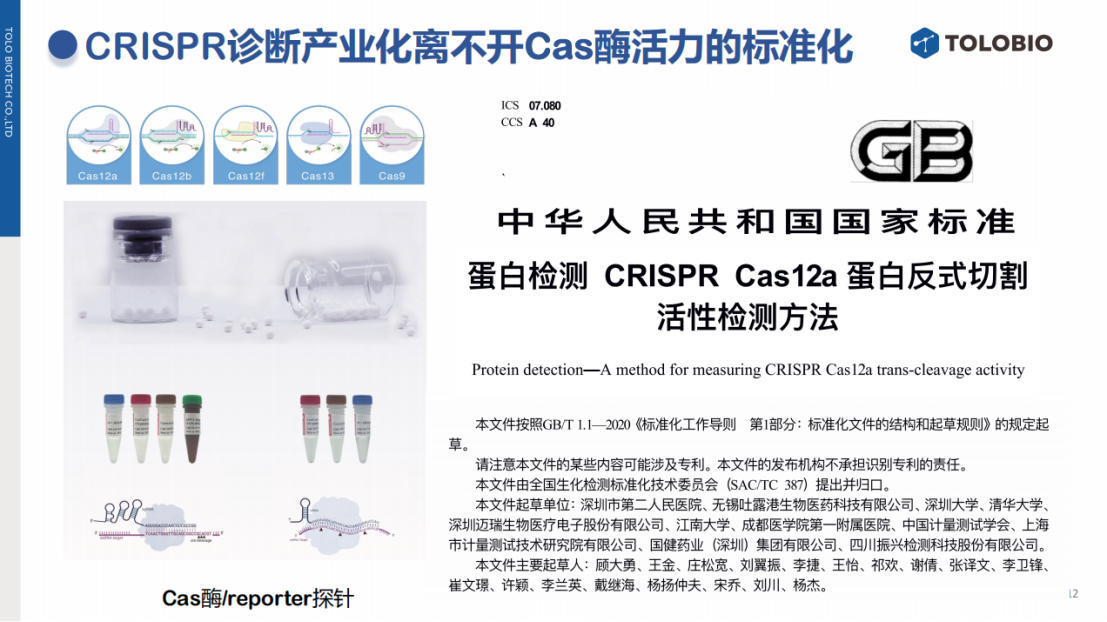
CRISPR技术从实验室走向产业化,标准化是关键。其中,核心原料——Cas蛋白的活性单位定义尤为突出。目前,行业内不同实验室或厂家提供的Cas蛋白浓度(µg/pM)相同但比活力可能存在巨大差异,导致实验结果难以重复。
4.2 标准化进展
为解决这一问题,吐露港生物联合了多家单位,推动起草了Cas蛋白(如Cas12a)反式切割活性的国家标准,建立酶活性单位(transU)计量体系,实现 Cas 酶原料的标准化供应,从而保证不同团队或不同企业间实验结果的可靠性和可重复性,加速CRISPR诊断技术的规范化和应用推广。
大家如果感兴趣,欢迎扫描二维码申请试用标准化的CRISPR-Cas酶。
同时,如有任何问题,可随时联系吐露港生物的技术顾问。期待大家的反馈!



发表评论 取消回复