我们从产品角度,概览当前IVD行业产品的整体构成情况


IVD行业发展过程中,产品同质化成为行业发展中的瓶颈问题。想要了解产品同质化情况,首先要对行业整体有初步了解。本期,我们从产品角度,概览当前IVD行业产品的整体构成情况。并对分子检测产品做进一步剖析,以期让关注行业全景的同仁对相关领域有更加清晰的全景认知。
根据DataMed数据库,参考官方分类标准,当前国内获批的IVD试剂产品可分为以下7类:
免疫法
化学法
辅助试剂(包括质控品、校准品等辅助检测试剂)
核酸检测
生物学检测(包括微生物培养与药敏等相关检测)
分离纯化检测(包括电泳、色谱、质谱等检测)
形态学检测(包括免疫组化、尿液有形成分分析等检测)
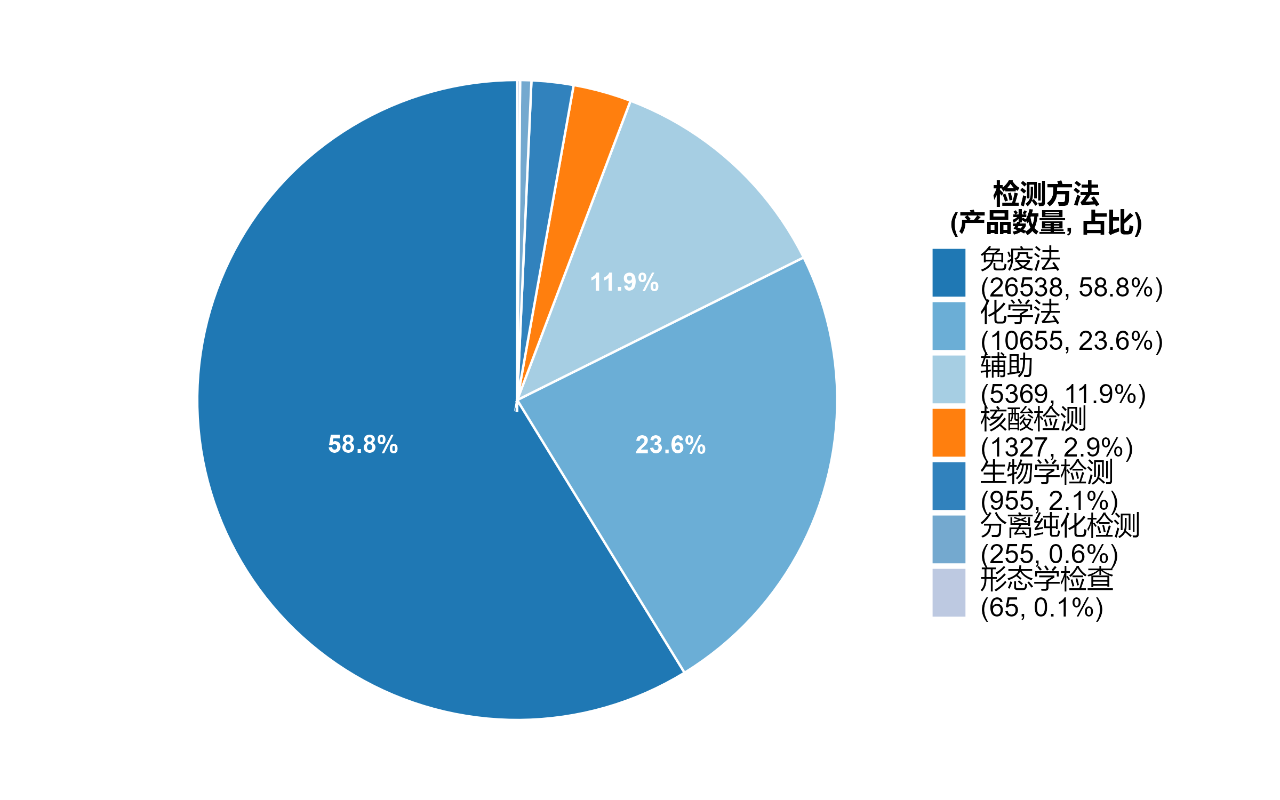
图1 展示了 NMPA批注的Ⅱ、Ⅲ类体外诊断试剂中,以上7类检测方法的数量及占比。合计产品数量约45164款,其中免疫学方法相关产品数量最多,占比达58.8%。
本期我们围绕1327款核酸检测产品,分析其技术路线演进及应用领域情况。并结合病原体核酸检测这一最大应用领域绘制产品竞争图谱。
1、时间发展特点:
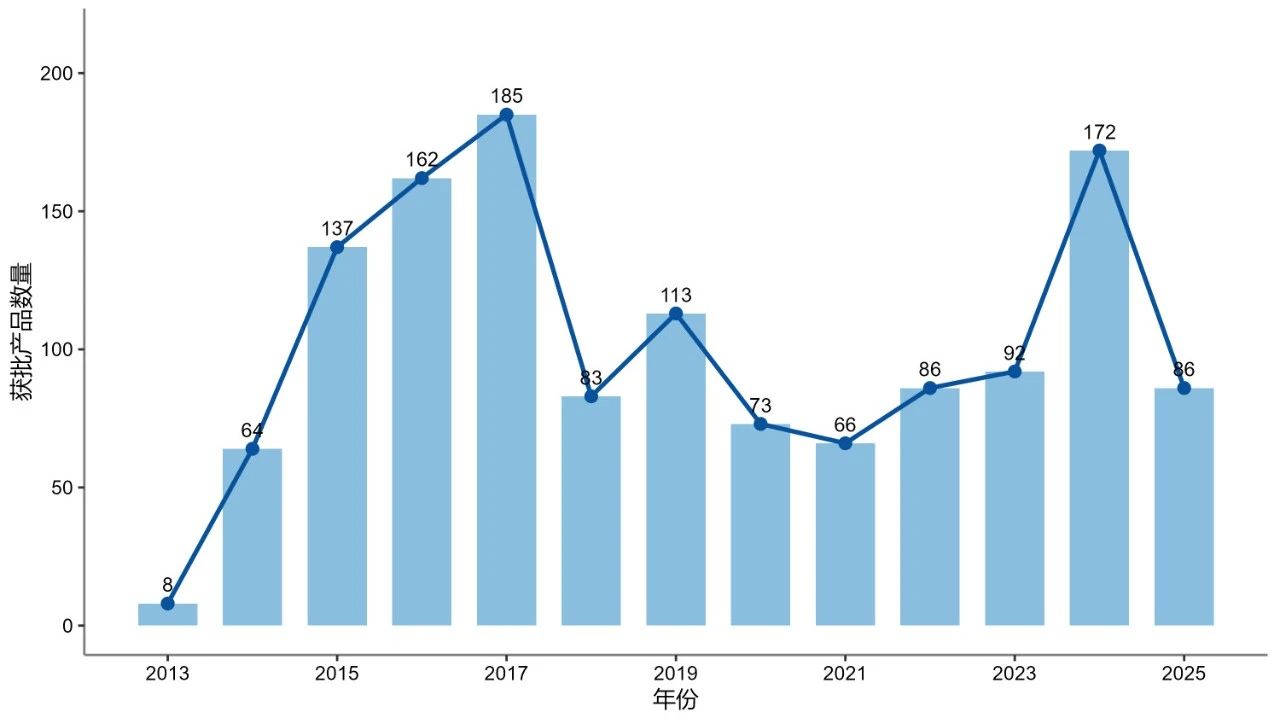
图2 展示了2013-2025年国内核酸检测产品获批数量的变化,从图中可见,2013—2017年间,核酸检测产品获批数量逐渐增加,并在2017年达到顶峰。随后获批数量下降,并在2024年再次达到获批数量顶峰。
2、技术路线发展特点:
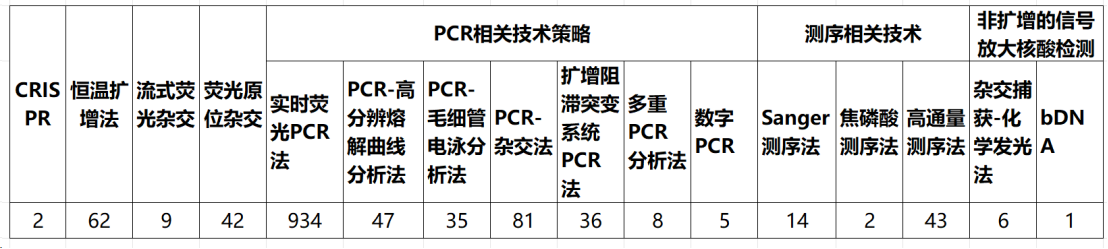
如表1所示,国内核酸检测产品共涉及实时荧光PCR、一代测序、高通量测序、非扩增的信号放大核酸检测、CRISPR、恒温扩增、荧光原位杂交等共计约16类分子检测技术,其中以实时荧光定量PCR检测技术获批产品数量最多,达934款。
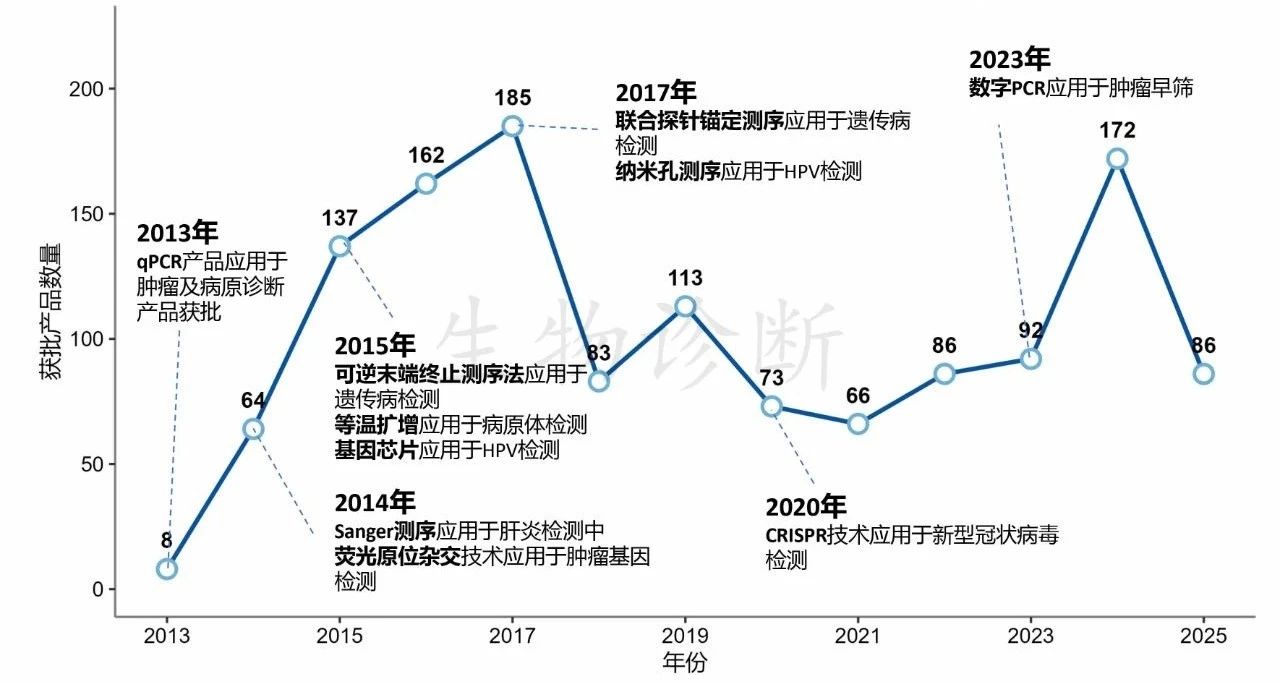
从技术演进路径上看(图2),按照相关试剂盒初始获批年份,呈现qPCR(2013年)→Sanger测序、荧光原位杂交(2014年)→可逆末端终止测序法、等温扩增、基因芯片(2015年)→联合探针锚定测序、纳米孔测序(2017年)→CRISPR(2020年)→数字PCR(2023年)的演进路径。
3、产品应用领域特点:
如图3所示,国内核酸检测产品主要的应用领域包括:
病原体核酸检测(829款产品)
药物基因组学(167款产品)
肿瘤靶向用药与预后评估(162款产品)、遗传性疾病基因检测(124款产品)
肿瘤早筛基因检测(43款产品)
肿瘤组织起源基因检测(1款产品)
自身免疫性疾病基因检测(1款产品)
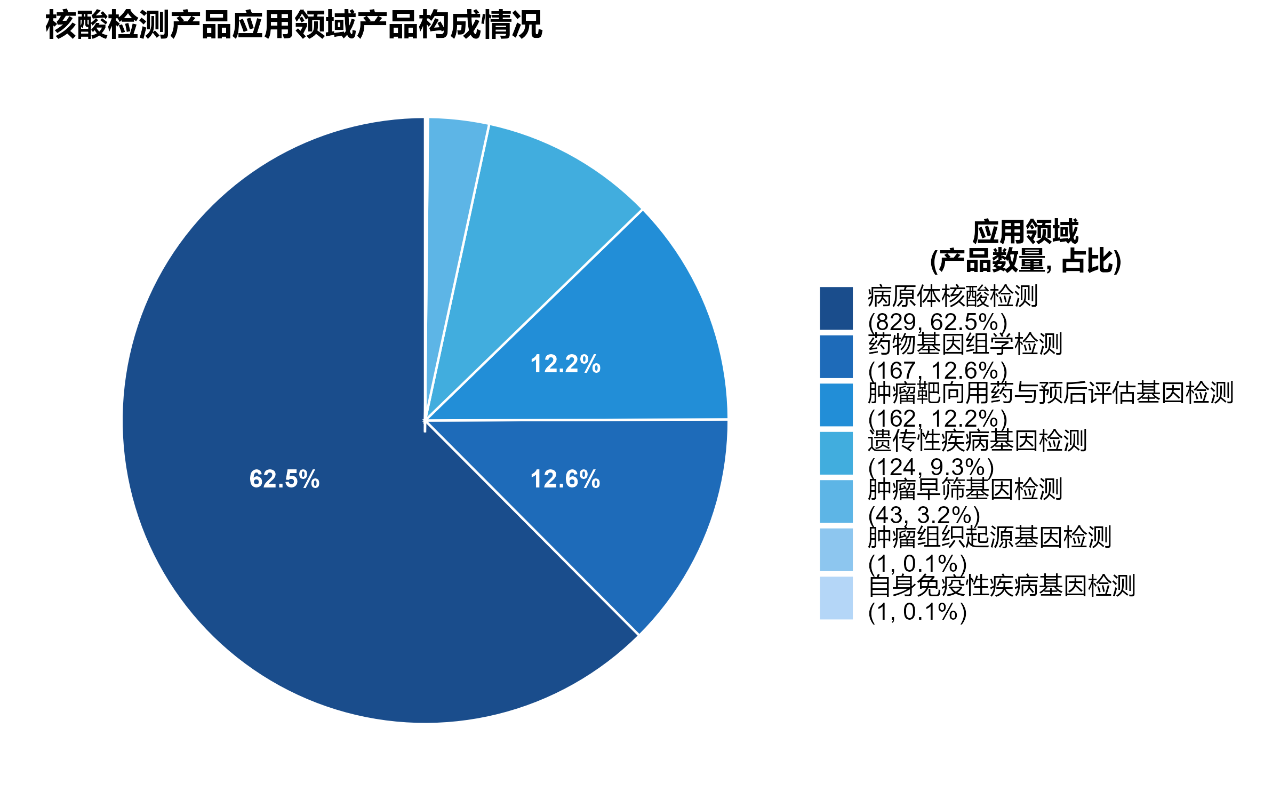
图3 核酸检测产品应用领域产品构成情况
4、病原体核酸检测靶标特点:
根据病原体检测靶标数量,当前病原单检产品数量约681款,联检产品数量约148款。
本次仅针对病原单检产品靶标情况做统计。欢迎后续持续关注。
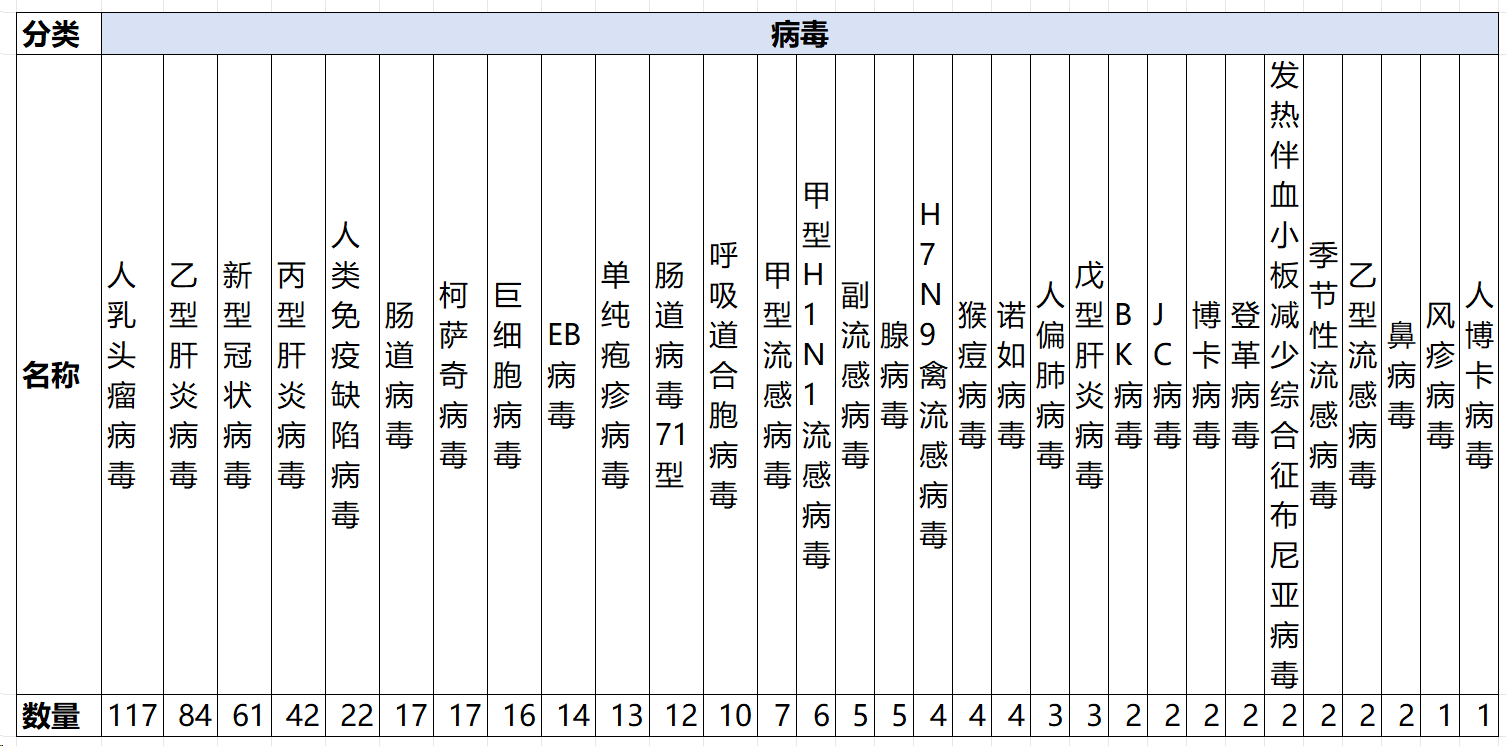
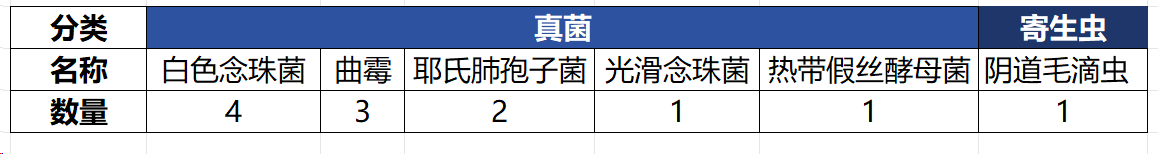
如下表2及图4所示,国内病原核酸单检产品覆盖病毒、细菌、真菌及寄生虫共计约59种病原体。
其中以人乳头瘤病毒、肝炎病毒、新型冠状病毒、人类免疫缺陷病毒、结核分枝杆菌单检产品数量最多。
笔者在以往文章中曾围绕几类重点病原体做过系统盘点,详细可关注:
幽门螺杆菌:国内幽门螺杆菌检测产品格局与趋势概览
HIV:国内 HIV 检测产品格局概览
结核分枝杆菌:270万病例未被及时发现!结核筛查有哪些新方向?
从WHO 2025 结核诊断指南,分析国内结核检测产品现状等
表2 不同检测靶标的单检病原体核酸检测产品获批数量概览






发表评论 取消回复